 1. Вода — единственное химическое вещество, которое широко распространено в естественных условиях на поверхности Земли во всех трех агрегатных состояниях: жидком, твердом и газообразном.
1. Вода — единственное химическое вещество, которое широко распространено в естественных условиях на поверхности Земли во всех трех агрегатных состояниях: жидком, твердом и газообразном.
2. Общеизвестно, что примерно 71% земной поверхности покрыто океанами, в которых содержится около 96,5% всей воды на планете, или 1,4 × 1018 тонн. Остальная вода на поверхности сохраняется в полярных льдах, горных ледниках, в реках и озерах, а также в подземных источниках и резервуарах.
3. Гораздо менее известно, что такое же, если не большее количество воды находится глубоко в мантии Земли, причем в основном не в виде молекул H2O, а в кристаллической решетке номинально безводных мантийных минералов в виде дефектов, состоящих из ионов Н+ или ОН–.
4. Озеро Байкал — самый большой резервуар пресной воды на планете: 23 600 км3. Озеро Верхнее — наибольшее в системе Великих озер Северной Америки — в два раза уступает Байкалу по объему (11 600 км3), но зато в 2,5 раза больше Байкала по площади и является в этом смысле самым большим пресноводным озером на Земле.
5. Как и у большинства жидкостей, плотность воды при охлаждении увеличивается. Однако, в отличие от большинства жидкостей, плотность замерзшей воды — льда — меньше, чем плотность жидкой воды в равновесии с этим льдом. Такое аномальное поведение приводит к наличию максимума плотности воды при температуре около 4 оС, что чрезвычайно важно для жизни на Земле. Если бы вода была наиболее плотной при замерзании, то зимой озера и реки промерзали бы не от поверхности вглубь, а от дна к поверхности, при этом погибала бы вся плавучая живность.
6. Известно около 18 кристаллических модификаций льда — тоже своеобразный рекорд. Ученые до сих пор открывают всё новые твердые фазы Н2О и спорят об их точном числе. Некоторые из этих структур льда устойчивы только при очень высоких давлениях и не плавятся даже при 1000 оС, если давление превышает несколько сотен тысяч атмосфер.
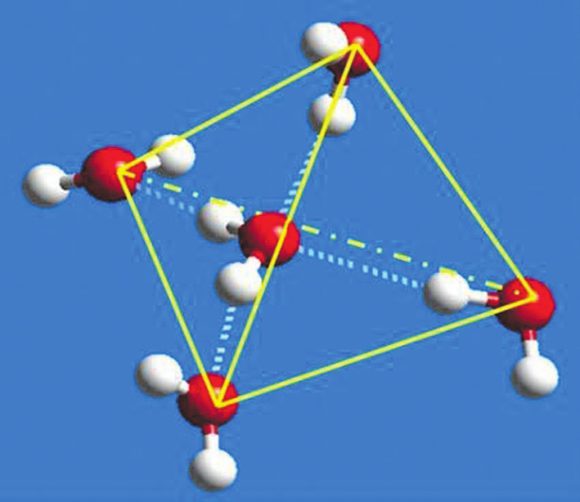
7. Многие аномальные свойства воды объясняются наличием водородных связей между ее молекулами. Структура отдельной молекулы воды — Н2О — довольно проста: вследствие гибридизации молекулярных орбиталей две составляющие ее О—Н связи (каждая — длиной около 0,1 нанометра) расположены друг к другу под углом примерно 104°. Близость этого угла к тетраэдрическому (109,5°) и характерное неравномерное распределение электронной плотности внутри молекул Н2О позволяет им легко образовывать водородные связи (Н-связи) со своими четырьмя ближайшими соседями. Атомы водорода выступают при этом донорами, а атом кислорода служит акцептором в среднем двух таких связей. Молекулы воды, связанные такими сетками Н-связей, образуют трехмерные структуры, представляющие собой более или менее крупные фрагменты локально упорядоченной алмазоподобной тетраэдрической кристаллической решетки (см. рис.). В кристалле обычного льда такая решетка близка к идеальной, а в жидкой воде при нормальных условиях структура этих небольших тетраэдрических молекулярных кластеров может быть искажена и быстро меняется со временем.
8. Энергия даже самых сильных водородных О···Н связей между молекулами в 10 раз слабее энергии составляющих отдельную молекулу ковалентных О—Н связей, поэтому трехмерная сетка Н-связей в воде постоянно разрывается и реорганизуется в новые похожие структуры просто в результате теплового движения молекул. Время жизни одной Н-связи очень коротко — всего порядка пикосекунды (10–12 с). Таким образом, об особой структуре воды и о «памяти воды» можно говорить, только имея в виду их крайнюю недолговечность.
9. С другой стороны, энергия водородных связей между молекулами Н2О гораздо выше энергии обычных межмолекулярных взаимодействий. Это приводит к так называемому гидрофобному эффекту, когда молекулы, которые слабо взаимодействуют с водой, склонны собираться вместе, минимизируя таким образом поверхность контакта (капельки масла в воде) и давая возможность молекулам Н2О создавать наибольшее количество Н-связей.
10. Внутримолекулярные и межмолекулярные водородные связи и гидрофобный эффект обеспечивают также особые структуру и функции трех важнейших типов макромолекул в живой природе: протеинов, нуклеиновых кислот и углеводов. Так, двойная спиральная структура молекулы ДНК чрезвычайно устойчиво сохраняется благодаря водородным связям между отдельными комплементарными нуклеотидами — элементами структуры ДНК, где в качестве акцептора Н-связи выступают не только атомы кислорода, но и атомы азота.
Андрей Калиничев


 (2 оценок, среднее: 3,50 из 5)
(2 оценок, среднее: 3,50 из 5)
«Как и у большинства жидкостей, плотность воды при охлаждении увеличивается».
Вы уверены? Вот прям-таки всегда-всегда увеличивается?:)
Ну, если написано, что имеется минимум, то, наверное, не прям-таки всегда-всегда.
Ой, неосторожное заявление, это точно
Не плотность увеличивается, а стоимость. К удельной стоимости воды прибавляется стоимость дров, потраченных на ее охлаждение.
«…благодаря водородным связям между отдельными комплементарными аминокислотами — элементами структуры ДНК…»
Может быть не аминокислотами, а нуклеиновыми кислотами или нуклеотидами?
Да, конечно. Сразу выдает в авторе не-биолога, не биохимика, и даже не органического химика вообще ;-)
Да уж, что-то легкомысленное…
Не про все интересные свойства воды рассказано. Например про то, что Земная вся вода имеет инопланетное происхождение, т.е. доставлена на Землю в виде огромных ледяных глыб откуда-то из космоса и точность стрельбы этими глыбами по планете Земля миллионами лет была уникальной. Или про то, что вода сконструирована так, что размеры её молекул примерно соответствуют размерам молекул углекислого газа, что сделало возможной фотосинтез растительности и развитие растительной жизни. Или про то, что вся земная вода уже используется по четвёртому циклу в составе растений и животных