Серию публикаций «10 фактов о…» продолжает доктор физ.-мат. наук, сотрудник Университета Мартина Лютера (Халле, Германия) Алексей Крушельницкий.
1. Белки — это линейные полимерные молекулы, состоящие из последовательности аминокислотных остатков. Хотя в живой природе существуют десятки различных аминокислот и многие из них могут входить в состав белков, основными являются двадцать непосредственно кодируемых в ДНК (см. п. 3). Каждая из аминокислот имеет одну и ту же химическую группу, которая при полимеризации образует пептидную связь (это вид амидной связи, которая образуется при взаимодействии группы — NH2 одной аминокислоты с группой — COOH другой) с соседними аминокислотами в линейной полипептидной цепи, и специфическую боковую цепь, которая отличает одну аминокислоту от другой.
2. Особенностью белков, отличающей их от большинства других природных и синтетических полимеров, является то, что все молекулы одного белка свернуты в одну и ту же строго определенную пространственную структуру (конформацию). Из этого правила есть исключения, но их очень немного.
3. В живой клетке белки синтезируются в сложном макромолекулярном комплексе, который называется рибосома. Для работы рибосомы необходимы отдельные аминокислоты, растворенные в цитоплазме клетки, и молекула рибонуклеиновой кислоты (РНК), в нуклеотидной последовательности которой закодирована аминокислотная последовательность того или иного белка (ну-клеотид — элементарное звено в линейной цепи ДНК и РНК). Каждой из 20 аминокислот соответствует свое сочетание из трех соседних нуклеотидов в РНК. Таким образом, рибосома протягивает через себя цепочку РНК, «считывает» ее нуклеотидную последовательность, в зависимости от комбинации нуклеотидов, захватывает из окружающего раствора ту или иную аминокислоту, связывает ее пептидной связью с предыдущей аминокислотой в цепочке и так далее, пока на РНК не кончится участок, кодирующий аминокислотную последовательность.
4. После выхода из рибосомы полипептидная цепь складывается в свою нативную пространственную структуру за время порядка одной секунды. И это весьма удивительно. Дело в том, что полипептидная цепь обладает очень большим числом степеней конформационной свободы. Если нативную структуру (которая, согласно базовым законам физики, должна обладать минимальной энергией) искать простым перебором всех возможных конформаций и при этом на каждую конформацию тратить время порядка одной пикосекунды (т.е. 10-12 с), то на поиск нужной конформации не хватит даже времени жизни Вселенной. Природа управляется с этим процессом намного быстрее.
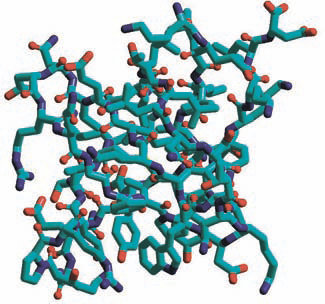
5. Пространственная структура белка определяется его аминокислотной последовательностью. Несмотря на интенсивные исследования, учеными пока не разработано метода, который бы позволял во всех случаях безошибочно предсказывать структуру белка по его аминокислотной последовательности.
6. Длина цепи для разных белков может различаться на порядки величин. Самые маленькие белки (к ним более применимо название олигопептиды) состоят из 15-20 аминокислотных остатков, а самые большие белки насчитывают много тысяч остатков. Белки очень сильно различаются не только по размеру, но и по своей биологической функции. Есть белки-ферменты, регуляторы, супрессоры, транспортные белки, рецепторы, структурные белки и т.д. Следует отметить, что есть много белков, функция которых в живых организмах пока неизвестна.
7. Условно белки можно поделить на три класса. Во-первых, это глобулярные белки. Они обычно имеют компактную структуру (глобулу), растворимы в воде и функционируют в жидкой среде. Во-вторых, это мембранные белки, которые находятся и работают на поверхности и/или внутри биологических мембран. В-третьих, это фибриллярные белки,нерастворимые в воде, которые образуют длинные волокна (фибриллы), служащие основой для мышечных и соединительных тканей, типичный пример такого белка — коллаген.
8. Хотя большинство белков имеет строго определенную структуру, эта структура не является абсолютно жесткой, она обладает определенной степенью конформационной подвижности. Эта подвижность крайне важна для биологической функции белков. Природа сконструировала белки таким образом, что хаотическая тепловая энергия окружающего раствора преобразуется в белке в целенаправленные молекулярные движения полипептидной структуры, без которых во многих случаях белки бы не работали.
9. В настоящее время существует только два экспериментальных метода, которые позволяют определять пространственную структуру белка, — рентгено-структурный анализ(РСА) и метод ядерного магнитного резонанса (ЯМР). В РСА монокристалл белка (не все, но многие белки могут образовывать кристаллы) облучается рентгеновскими лучами, которые после прохождения через образец дают дифракционную картину. По этой картине с помощью сложных расчетных методов восстанавливается структура белка. В эксперименте ЯМР измеряется сила магнитных взаимодействий между магнитными ядрами, которая зависит от расстояния между ними. Структура макромолекулы определяется также с помощью сложных компьютерных алгоритмов, по измеренным таким образом межъядерным расстояниям.
10. Благодаря развитию генной инженерии для исследований сейчас часто используются так называемые рекомбинантные белки. Для их получения модифицируется геном (ДНК) бактерий для того, чтобы они синтезировали нужный исследователям белок в больших количествах. Основное преимущество этого метода по сравнению с выделением природных белков из живых организмов — в том, что он позволяет относительно легко получать мутантные белки (т.е. белки с измененной аминокислотной последовательностью), а также белки с изотопным обогащением. Таким же образом производятся многие белки, широко применяемые в медицине в качестве лекарств (инсулин, эритропоетин, факторы роста и др.).