Как известно, каждый человек — это суперорганизм, сообщество, состоящее из самого этого человека и множества живущих в нем и на нем бактерий. Количество бактериальных клеток на несколько порядков превосходит количество клеток самого человека, а их суммарный вес составляет два-три килограмма.
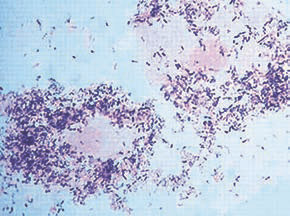
Большинство бактерий живет в кишечнике, но не только. Анализ бактериальных сообществ, живущих на коже человека, показал существование трех существенно различных типов микрофлоры: на влажной коже (например, подмышками или в пупке), на сухой коже (например, на плече или на локте) и на жирной коже (лоб между бровями, крылья носа, канал уха и т.п.) [1]. Области с жирной кожей характеризуются наименьшим разнообразием видов, в основном Propionibacteria и стафилококков. Впрочем, в другом исследовании было показано, что использование косметики, в частности пудры, существенно увеличивает разнообразие бактерий на лбу [2]. Следует отметить, что эти исследования имеют не только косметическое значение: так, агрессивный штамм лекарственно-устойчивого Staphylococcus aureus приобрел гены, дающие ему возможность жить на коже, горизонтальным переносом от обычного компонента нормальной микрофлоры S. epidermidis [3].
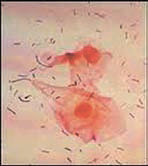
Еще больший медицинский интерес представляет микрофлора слизистых оболочек, в частности, половых путей. В вагине здоровых женщин живут различные виды лактококков, причем доля женщин с преобладанием тех или иных видов лактококков зависит от этнической группы (белые, азиатки, афроамериканки и латиноамериканки); кроме того, у двух последних групп часто встречаются сообщества, в основном состоящие не из лактококков, а из строгих анаеробов (превотелл, гарднерелл и т.п.), впрочем, также производящих молочную кислоту [4]. В зависимости от преобладающего типа вагинальных сообществ различалась и кислотность: у латиноамериканок (pH 5.0 ± 0.59) и афроамериканок (pH 4.7 ± 1.04) она была значимо выше, чем у азиаток (pH 4.4 ± 0.59) и белых (pH 4.2 ± 0.3). Наблюдаемые различия могут быть связаны как с генетическими особенностями хозяев (иммунный статус, состав лигандов на поверхности эпителия и т.д.), так и с особенностями стиля жизни: диеты, гигиенических привычек, способов контрацепции, полового поведения и т.п. Одним из практических выводов из этой работы является то, что следует пересмотреть клинические (микробиологические) критерии нормальности вагинальной микрофлоры: они должны учитывать этническую принадлежность пациенток, поскольку при существующих критериях абсурдно большой доле афроамериканок и латиноамериканок должен быть диагностирован дисбактериоз при полном отсутствии клинических симптомов.
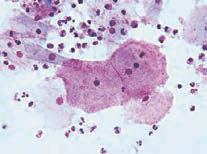
Бактериальный вагиноз является фактором риска при опасности заражения ВИЧ. Анализ вагинальной микрофлоры 132 ВИЧ-положительных женщин из Танзании показал, что гарднереллы и лактобациллы присутствуют во всех сообществах, причем лактобациллы являются признаком нормальной микрофлоры,а вагиноз ассоциирован с превотеллами и Lachnospiraceae [5]. При этом, видимо, превотеллы являются фактором риска не потому, что они сами являются потенциальными патогенами, а поскольку они производят метаболиты (аммоний, аминокислоты), потребляемые патогенами Gardnerella vaginalis и Peptostreptococcus anaerobius [6-7]. В похожем исследовании, проведенном в Китае, сравнивали 50 здоровых женщин и 50 женщин, больных вагинозом [8]. В то время, как единого маркера для здоровых сообществ обнаружено не было, три типа (Bacteroidetes, Actinobacteria, Fusobacteria) и восемь родов, в том числе и уже упоминавшихся (Gardnerella, Atopobium, Megasphaera, Eggerthella, Aerococcus, Leptotrichia/Sneathia, Prevotella, Papillibacter), значимо чаще наблюдались у больных вагинозом по сравнению со здоровыми контролями.
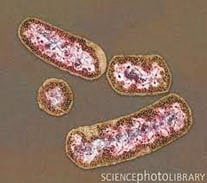
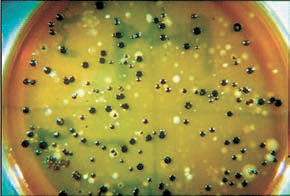
Впрочем, исследователи изучают не только вагинальную микрофлору самок человека. Было показано, что, несмотря на анатомическое и физиологическое сходство репродуктивных органов человека и бабуина, их микрофлора существенно различна: хотя у самок бабуинов, как и у человека, преобладают Грам-положительные бактерии (Firmicutes), но это не лактобациллы; некоторые группы Грам-отрицательных бактерий встречаются у бабуинов, но не у человека [9]. С другой стороны, анализ микрофлоры уретры мужчин показал, что некультивируемые бактерии, ассоциированные с вагинальными патологиями, часто встречаются у асимптоматических носителей, не имеющих признаков воспаления уретры [10]. При этом асимптоматическое носительство возбудителей заболеваний, передающихся половым путем (хламидии и гонококки), коррелировало с наличием уже знакомых маркеров вагиноза: Sneathia, Gemella, Aerococcus, Anaerococcus, Prevotella, Veillonella.
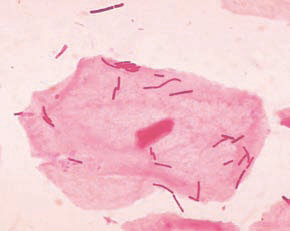
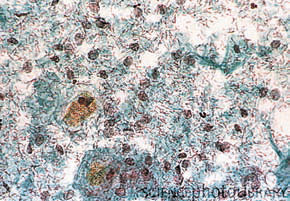
Ясно, что все это — только первый, очень поверхностный взгляд на бактериальные сообщества, живущие на и в человеке. Ясно также, что технологический прогресс позволит сделать такого рода исследования рутинными, и в конечном счете полный список бактерий — с оценками численности — станет обычной частью стандартного клинического анализа. Помимо «вообще» больных и «вообще» здоровых будут сопоставлены различные варианты течения болезней, стадии заболеваний, ответ на лечение антибиотиками. Будут определены условия, при которых общераспространенные бактерии становятся патогенами. Болезни будут разделены не только по внешним клиническим проявлениям, но и по детальному микробиологическому портрету, и лечение будет индивидуализировано в зависимости от этого портрета — нечто подобное начинает происходить с раком.
М.Г.
1. Grice EA et al. Topographical and temporal diversity of the human skin microbiome. Science 324: 1190 (2009).
2. Staudinger T et al. Molecular analysis of the prevalent microbiota of human male and female forehead skin compared to forearm skin and the influence of make-up. J. Appl. Microbiol. 110: 1381 (2011).
3. Diep BA et al. Complete genome sequence of USA300, an epidemic clone of community-acquired meticillin-resistant Staphylococcus aureus. Lancet 367: 731 (2006).
4. Ravel J et al. Vaginal microbiome of reproductive-age women. Proc. Natl. Acad. Sci. USA 108: 4680 (2011).
5. Hummelen R. Deep sequencing of the vaginal microbiota of women with HIV. PLoS One 5: e12078 (2010).
6. Pybus V, Onderdonk AB. Evidence for a commensal, symbiotic relationship between Gardnerella vaginalis and Prevotella bivia involving ammonia: Potential significance for bacterial vaginosis. J. Infect. Dis. 175: 406 (1997).
7. Pybus V, Onderdonk AB. A commensal symbiosis between Prevotella bivia and Peptostreptococcus anaerobius involves amino acids: Potential significance to the pathogenesis of bacterial vaginosis. FEMS Immunol. Med. Microbiol. 22:317 (1998).
8. Ling Z et al. Molecular analysis of the diversity of vaginal microbiota associated with bacterial vaginosis. BMC Genomics 11: 488 (2010).
9. Rivera AJ et al. Differences between the normal vaginal bacterial community of baboons and that of humans. Am. J. Primatol. 73: 119 (2011).
10. Nelson DE et al. Characteristic male urine microbiomes associate with asymptomatic sexually transmitted infection. PLoS ONE 5: e14116 (2010).
